Presentación del Proyecto Final Química Ort 2008
Proyecto Química ORT del Genoma Humano
(Notese que el blog comienza abajo de todo, y cada nuevo dia se va poniendo encima del otro, quedando el final arriba)
Por cuarto año consecutivo los alumnos del último año de la especialidad Química de la Escuela Técnica ORT Argentina realizarán sus proyectos finales en distintas universidades y centros de investigación con profesionales reconocidos. La metodología de trabajo evita la transpocisión didáctica permitiendo a los estudiantes realizar su actividad final en los lugares donde se está generando el conocimiento.
La articulación entre el nivel medio y el postgrado universitario es auspiciada por el CONICET (Consejo Nacional de Investigaciones Científicas y Técnicas). Los 15 proyectos de investigación (incluyendo este) para el año en curso son:
Nuestro Proyecto: Estudio de la Growth Associated Protein (GAP-43), su interacción con la Ubicutina y su participación en el control del ciclo celular en células NIH3T3 transfectadas en forma estable y transiente. Efecto de la Apo-transferrina en la remielización: participación de la vía Notch en la diferenciación oligodendrioglial.
Investigador: Doctora Ana María Adamo
Instituto: Departamento de Química Biológica Patológica, Facultad de Farmacia y Bioquímica de la UBA. CONICET.
Alumnos: Rodrigo C. Pampin y Robby Mattes
1) Proyecto: Evaluación de la expresión de la molecula de adhesión cadherina epitelial en tejidos humanos normales y tumorales.
Investigador: Dra. Mónica Vazquez-Levin.
Instituto: Instituto de Biología y Medicina Molecular (IBYME - CONICET).
Alumnos: Yael Dobzewicz Y Gala Szapiro.
Link: http://www.proyecto-6q.blogspot.com/
2) Proyecto: Acción del hexaclorobenceno (HCB) sobre la uroporfirinogeno de una línea celular hepatocitos humanos. Mecanismo de acción.
Investigador: Dra. María del Carmen Ríos de Molina. Instituto: Departamento Química Biológica, Facultad de Ciencias Exactas y Naturales.
Alumnos: Lucas Toiw y Uriel Frid.
Link: http://www.proyectofrid-toiw08.blogspot.com/
3) Proyecto: Modelos experimentales de enfermedades metabólicas: Porfiria y Síndrome Metabólico. Proteómica y Metabolómica de estos disturbios.
Investigador: Dra. Marta Blanca Mazzetti.
Instituto: Departamento de Química Biológica, Facultad de Ciencias Exactas y Naturales (UBA).
Alumnos: Maria Duperron y Mauro Elencwajg.
Link: http://proyectofinal6q.blogspot.com/
4) Proyecto: Factores no hemodinámicos relacionados con la génesis y evolución de la proteinuria durante la enfermedad renal progresiva.
Investigador: Dra. Elsa Zotta.
Instituto: Laboratorio de Fisiopatogénia, Departamento de fisiología, Facultad de medicina, UBA.
Alumnos: Barbara Helueni y Melanie Naiman.
Link: http://www.proyectoq08.blogpsot.com/
5) Proyecto: Estudio de la participacion de la anandamida en la regulacion de la interaccion espermatozoide-ovioducto en un modelo bovino.
Investigador: Dra. Silvina Perez Martinez.
Instituto: Facultad de medicina - UBA
Alumnos: Judith Arenas Tenenbaum y Melina Braverman
Link: http://www.scienceproject08.blogspot.com/
6) Proyecto: El estudio de los mecanismos moleculares involucrados en la regulación del gen UGA4 de Saccharomyces cervisiae en respuesta a cambios en la disponibilidad de nutrientes con el fin de dilucidar las distintas cascadas de señales desencadenadas por dichos nutrientes y establecer sus interconexiones.
Investigador: Dra. Susana Correa García.
Instituto: Departamento de Química Biologica, Facultad de ciencias Exactas y Naturales, Universidad de Buenos Aires.
Alumnos: Iván Mikiej y Victoria Salama
Link: http://www.proyectoquimica22.blogspot.com/
7) Proyecto: Diagnóstico de la enfermedad de Von Willebrand (VWD) tipo 2N por técnicas fenotípicas y genotípicas.
Investigador: Dra. Adriana I. Woods.
Instituto: Instituto de Investigaciones Hematológicas "Mariano R. Castex" de la Academia Nacional de Medicina.
Alumnos: Abigail Skverer y Daniela Lin
Link: http://www.vwd-diagnostico.blogspot.com/
8) Proyecto: Estudio de la mielinogenesis en el sistema nervioso periferico en condiciones fisiologicas y patologicas. Participacion de celulas pluripotentes en el proceso de degeneracion-regeneracion nerviosa.
Investigador: Dra Patricia Setton-Avruj.
Instituto: Dpto de Quimica Biologica, Facultad de Farmacia y Bioquimica (IQUIFIB-UBA-CONICET).
Alumnos: Daniel Averbuj y Eitan Rozenszajn.
Link: http://www.proyectoaverbuj-rozenszajn.blogspot.com/
9) Proyecto: Diseño y desarrollo de vacunas antitumorales empleando bacterias y celulas tumorales modificadas con genes inmunomodiladores. Estudio de los mecanismos inmunes inducidos.
Investigador: Claudia I. Waldner y Claudia Mongini.
Instituto: Laboratorio de inmunologia celular y molecular. Centro de Estudios Farmacologicos y Botanicos (CEFYBO. CONICET-UBA)
Alumnos: Amalia Surijon y Maria Belen Tolava Rivero
Link: http://www.amibeluproyecto.blogspot.com/
10) Proyecto: Marcadores Geneticos Asociados al Cáncer
Investigador: Dr.Javier Hernán Cotignola
Instituto: Laboratorio de Cáncer y Apoptosis del Departamento de Quimica Biologica de la Facultad de Ciencias Exactas y Naturales de la Universidad de Buenos Aires.
Alumnos: Ayelén Marano y Solange Perchik
Link: http://marcadoresgeneticos.blogspot.com/
11) Proyecto: Expresion del canal de la conductancia transmembranal de la Fibrosis Quistica (CFTR) en placentas Preeclampticas: posible rol en la regulacion de la actividad de la Acuoporina-9 (AQP9).
Investigador: Dr Alicia E Damiano
Instituto: Catedra de Biologia Celular, Departamento de Ciencias Biologicas, Facultad de Farmacia y Bioquimica (UBA)
Alumnos: Gabriel Colodenco y Martín Sapir.
Link: http://www.tarkuselp.blogspot.com/
12) Proyecto: Proteómica de factores secretados por células de cáncer de mama y mama normal con capacidad inhibitoria de la producción lipídica.
Investigador: Dra.Guerra de Grignoli Liliana Noemi
Instituto: Departamento de Ciencias biologicas. Facultad de ciencias exactas y naturales,UBA-CONICET.
Alumnos: Fabiana Durante y Tamara Broitman.
Link: http://tyf-proyecto08.blogspot.com/
13) Proyecto: Neovascularizaciòn en un modelo murino de inflamaciòn aguda inducida por LPS.
Investigador: Eulalia de la Torre.
Instituto: Facultad de Medicina - Uba - Laboratorio de Inmunofarmacologia
Alumnos: Federico Mauas Walach, Pablo Kuleff.
Link: http://finalproyectort.blogspot.com/
14) Proyecto: Interacción de sumo-1 y mage-a2 en la regulacion del oncosupresor p53.
Investigador: -
Instituto: -
Alumnos: Yair Litman y Leonel Sterman
Link: http://proyectosumo.blogspot.com/
martes, 25 de noviembre de 2008
Presentacón
Presentación del Proyecto Final Química Ort 2008
Día 17: Conclusión Final
Los resultados presentados en esta monografía demuestran que se cumplieron los objetivos propuesto. La visualización de los conjugados de ubicuitina es una tarea dificultosa y hasta el momento las técnicas generalmente utilizadas para la detección de los mismos incluyen inmunoprecipitación seguida de Western Blot utilizando anticuerpos específicos. Esta técnica tiene limitaciones ya que no permite el análisis de la ubicuitinización en células in vivo.
La técnica de fluorescencia por complementación desarrollada por Deyu Fang and Tom K. Kerppola es una herramienta útil para la visualización de proteínas ubicuitinizadas en células in vivo. Una vez puesto a punto este sistema, el mismo podrá ser utilizado para la localización de conjugados de ubicuitina de cualquier proteína de interés. Teniendo en cuenta los antecedentes del grupo de trabajo, este sistema podrá ser utilizado para caracterizar la conjugación de GAP-43 a la ubicuitina.
Además, cabe destacar que en esta monografía se utilizaron técnicas de biología molecular siendo esta una herramienta muy útil para el estudio y compresión de diversos procesos celulares.
Día 16: Resultados de la tranfección
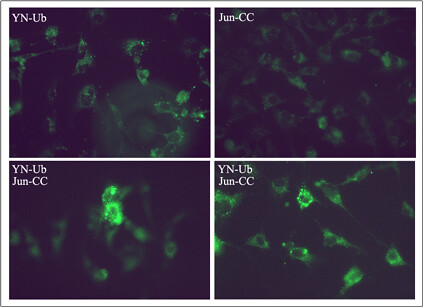
Se pudo obtener una visualización directa de los conjugados de Jun con ubicuitina en las células transfectadas con las distintas construcciones. Como se puede observar en la imagen de la figura 4, las células transfectadas con ambos plásmidos son fluorescentes y sorprendentemente esta fluorescencia se observa principalmente en pequeñas estructuras citoplasmáticas, visualizadas como un puntillado. La localización de estas estructuras es perinuclear. Por otro lado, las células transfectadas con los plásmidos solos no muestran una fluorescencia marcada y la distribución de la misma es diferente a la de las células cotransfectadas.
Este resultado confirma la factibilidad de la metodología, la identificación de conjugados de Jun con ubicuitina en células “in vivo” y sugiere que la ubicuitinización de Jun causa un transporte de esta proteína nuclear hacia estructuras citoplasmáticas como fue descripto por Deyu y colaboradores.
Día 15: Transfección
El día anterior al experimento se sembraron 3000 células en placa de 24 pocillos conteniendo cubre objetos de vidrio previamente tratados con poly-L lisina. En el momento de la transfección, las células estuvieron en un 70-80 % de confluencia, fase exponencial del crecimiento de las mismas donde el ingreso del plásmido esta favorecido. Para cada pocillo se obtuvo una mezcla de transfección que constó en la preparación en forma separada de dos soluciones. En una de ellas se diluyó 1 mg de DNA (ya sea el plásmido YN-Ub o el Jun-CC) en 200 ml de medio libre de suero y antibiótico. La otra solución contenía 5ml de LipofectaminaTM 2000 diluida en 200 ml de medio libre de suero y antibiótico.

Ambas soluciones se dejaron reposar aproximadamente 15 minutos. Luego de la incubación se combina el ADN diluido con la solución de LipofectaminaTM 2000 para la formación de los complejos y se le adicionan 600 ml del medio sin suero y sin antibiótico (volumen final 1 ml). Se mezcló suavemente y se incubó durante 45 minutos a temperatura ambiente. Mientras tanto la monocapa de células se lavó con medio libre de suero y antibiótico y cumplido los 45 minutos se le agregó a cada pocillo los complejos.

Las células se incubaron en estufa en su forma habitual y 5 horas más tarde se les agregó a cada pocillo 1ml de medio conteniendo 20% de suero fetal bovino, penicilina 100 U/ml y estreptom
icina 100 mg/ml (2 x el medio completo). De esta manera, al entrar en contacto con el medio presente, este se diluyó a su concentración habitual. Al día siguiente se cambia el medio de cultivo y se incuba hasta cumplidas las 24 hrs. post-transfección. Posteriormente se incubaron las células 6 hrs. a 30ºC para poder observar la complementación de fluorescencia ya que esto favorece la maduración del fluoróforo. Una vez cumplido ese tiempo las células fueron fijadas con paraformaldehido 4% en PBS durante 20 minutos. Luego se procedió a lavados exhaustivos con PBS para eliminar restos de paraformaldehido y finalmente los cubreobjetos de vidrio fueron montados en portaobjetos con medio de montaje para fluorescencia (Dako). Las células se mantienen en oscuridad. Se observo la fluorescencia de las células transfectadas con microscopio de fluorescencia (Olympus Optical CO, LTD, Japón) y se capturó la imagen de las mismas ya que este posee una cámara acoplada Olympus BX50.

Día 14: Cuantificación del ADN
La cantidad total de ADN presente en las muestras de los plásmidos purificados se determinó midiendo la absorbancia de una alícuota de dichos plásmidos a 260 nm y a 280 nm con un espectrofotómetro. La absorbancia a 260 nm se empleó para calcular la concentración de ADN. Una solución de 50 μg/ml proporciona una absorbancia de 1, por lo que la concentración de ADN en la muestra en μg/ml es igual a 50 x A260 nm. El cociente de absorbancias 260/280 se utiliza para calcular la pureza de la preparación. Un cociente inferior a 1.8 indica que hay impureza.
| | 260nm | 280nm | 260/280 | Concentración |
| YN-Ub | 0,344 | 0,227 | 1.5 | 0.592 μg/μl |
| Jun-CC | 0,932 | 0,605 | 1.5 | 2.33 μg/μl |
Día 13: Midiprep
Se realizó una midiprep para la purificación del ADN utilizando un kit comercial de Wizard Plus Midipreps DNA Purification System (Promega) que permite un método de aislamiento rápido y confiable para el ADN. Una vez obtenido el ADN, se realizó una nueva digestión enzimática para realizar una electroforesis en geles de azarosa 1% para la cuantificación utilizando un estándar גHind III.
Aqui se puede observar el procedimiento de la midiprep.
